Download PDF For kinetic theory class 11 physics notes pdf - Physics Notes In Hindi
Kinetic Theory Class 11 Notes Physics Chapter 13
• गतिज सिद्धांत का विकास उन्नीसवीं शताब्दी में मैक्सवेल, बोल्ट्जमैन और अन्य लोगों द्वारा किया गया था। काइनेटिक सिद्धांत इस विचार के आधार पर गैसों के व्यवहार की व्याख्या करता है कि गैस में तेजी से गतिमान परमाणु या अणु होते हैं।
• Ideal Gas
एक आदर्श गैस या एक आदर्श गैस वह गैस है जो बॉयल के नियम, चार्ल्स के नियम, गे लुसैक के नियम आदि जैसे गैस कानूनों का कड़ाई से पालन करती है।
एक आदर्श गैस में निम्नलिखित विशेषताएं होती हैं:
(i) एक आदर्श गैस का अणु एक बिंदु द्रव्यमान होता है जिसमें कोई ज्यामितीय आयाम नहीं होता है।
(ii) गैस के अणुओं में कोई आकर्षण या प्रतिकर्षण बल नहीं होता है।
• Kinetic Theory and Gas Pressure
गैस का दबाव कंटेनर की दीवारों के खिलाफ गैस के अणुओं की निरंतर बमबारी का परिणाम है। गतिज सिद्धांत के अनुसार, एक आदर्श गैस द्वारा लगाया गया दबाव P द्वारा दिया जाता है
 |
| kinetic theory class 11 physics notes pdf |
kinetic theory class 11 physics notes pdf : Equation of State of an Ideal Gas
किसी गैस के दाब P, आयतन V और निरपेक्ष तापमान T के बीच के संबंध को उसकी अवस्था का समीकरण कहा जाता है। एक आदर्श गैस की अवस्था का समीकरण
PV = nRT
जहाँ n संलग्न गैस के मोलों की संख्या है और R दाढ़ गैस स्थिरांक है जो सभी गैसों के लिए समान है और इसका मान है
R = 8.315 JK-1 mob-1
• Avagadro’s Law
S.T.P. के तहत सभी गैसों की समान मात्रा। अणुओं की संख्या 6.023 x 1023 के बराबर होती है।
• Graham’s Law of Diffusion of Gases
इसमें कहा गया है कि गैस के विसरण की दर गैस के घनत्व के वर्गमूल के व्युत्क्रमानुपाती होती है।
 |
| class 11 physics notes in hindi |
• Kinetic Interpretation of Temperature
किसी गैस के सभी अणुओं की कुल औसत गतिज ऊर्जा उसके निरपेक्ष तापमान (T) के समानुपाती होती है। इस प्रकार, किसी गैस का तापमान गैस के अणुओं की औसत गतिज ऊर्जा 'IT' का माप होता है।
U = 3/2 RT
तापमान की इस व्याख्या के अनुसार, औसत गतिज ऊर्जा U, T = 0 पर शून्य है, अर्थात अणुओं की गति पूर्ण शून्य पर समाप्त हो जाती है।
• Degrees of Freedom
किसी अणु की स्थिति को निर्दिष्ट करने के लिए आवश्यक स्वतंत्र निर्देशांक की कुल संख्या या किसी भी अणु के साथ संभव गति के स्वतंत्र मोड की संख्या को स्वतंत्रता की डिग्री कहा जाता है।
मोनो-, डी-, और पॉलीएटोमिक (एन) अणुओं में स्वतंत्रता की डिग्री की संख्या 3,5 या (3 N-K) है जहां के बाधाओं की संख्या है [संरचना से जुड़े प्रतिबंध]।
• Law of Equipartition of Energy
थर्मल संतुलन में एक गतिशील प्रणाली के लिए, सिस्टम की ऊर्जा स्वतंत्रता की विभिन्न डिग्री के बीच समान रूप से वितरित की जाती है और प्रति अणु स्वतंत्रता की प्रत्येक डिग्री से जुड़ी ऊर्जा 1/2 kT है, जहां k बोल्ट्जमैन स्थिर है।
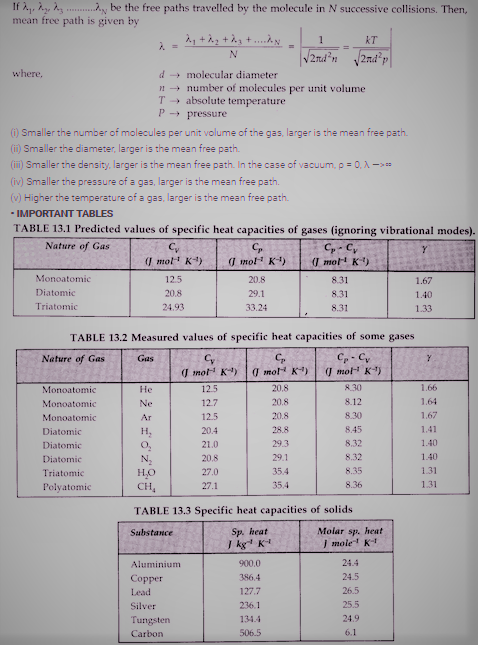
• Mean Free Path
किसी गैस में अणु का माध्य मुक्त पथ दो क्रमागत टक्करों के बीच अणु द्वारा तय की गई औसत दूरी है
 |
| physics class 11 chapter 13 notes |










No comments:
Post a Comment